Periyodik Tablo S Bloku Elementleri ve Özellikleri
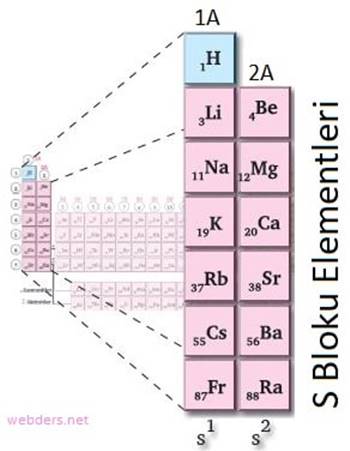
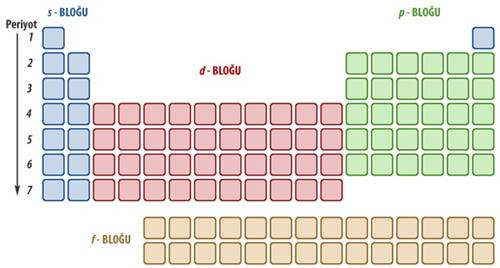
Periyodik tablo elementleri, benzer kimyasal özelliklere sahip oldukları için grup numaralarına göre sınıflandırılmaktadır. S bloku elementleri ise periyodik tablonun en solunda bulunan 1A ve 2A elementleridir. Bu grupların S blok elementleri olmasının sebebi ise değerlik orbitallerinin S orbitalleri olmasıdır. Diğer bir deyişle elektron dizilişleri s orbitaliyle biten elementlere S Bloku Elementleri denir.
Helyum elementi soygaz olduğu için 1A veya 2A grubuna değil 8A grubuna konulmuştur. Bu nedenle bazı yerlerde Helyum elementini P blok elementleri arasında görebilirsiniz. S blok elementleri grupları olan 1A grubuna alkali metaller, 2A grubuna ise toprak alkali metaller (alkalin) denilmektedir.
İlginizi Çekebilir: Periyodik Tablo 1A Grubu Elementleri
İlginizi Çekebilir: Periyodik Tablo 2A Grubu Elementleri
S blok elementleri küresel simetri bir yapıya sahiptirler. Çünkü s1 veya s2 ile sona erdikleri için tam dolu veya yarım doludurlar.
S Bloku Elementleri Hangileridir?
1A Grubu Elementleri: Hidrojen, Lityum, Sodyum, Potasyum, Rubidyum, Sezyum, Fransiyum.
2A Grubu Elementleri: Berilyum, Magnezyum, Kalsiyum, Stronsiyum, Baryum, Radyum.
8A Grubu Elementleri: Helyum.
Periyodik Tablo S Bloku Elementlerinin Özellikleri
1 – Periyodik tablodaki 1A ve 2A grubu elementleridir.
2 – Aynı periyottaki elementlere göre atom yarıçapları daha büyüktür.
3 – Atom hacimleri daha fazladır. Bunun sonucu olarak da yoğunlukları düşüktür.
4 – Hidrojen elementi hariç diğer bütün elementler metaldir.
5 – Metalik aktiflikleri yüksektir (yani tepkimeye girme eğilimleri yüksektir).
6 – Bileşiklerinde aldıkları değerler +1 ve +2’dir.
7 – Küresel simetri özelliklerine sahiptirler.
8 – 1A grubu elementleri en aktif metallerdir. Bu elementler hemen hemen her element ile tepkimeye girmek isterler. Bunun sonucu olarak da doğada saf halde bulunmazlar.
9 – Hidrojen elementi ametal, Helyum elementi ise bir soy gazdır.
10 – Helyum ve Hidrojen hariç diğer elementler metal oldukları için ısı ve elektrik iletimi, ametaller ile tepkimeye girme eğilimi yüksektir.
11 – Parlak bir görünüme sahiptirler.
12 – Hidrojen hariç diğer 1A grubu elementleri +1 iyon yükü ile yüklenirken 2A grubu elementleri +2 iyon yükü ile yüklenirler.
13 – Helyum elementini S blok elementi olarak varsayarsak bu element, elektron alıp vermez. Çünkü soy gazlar kararlı bir yapıya sahiptirler.
14 – Aktif olan metaller hemen Oksijen elementi ile tepkimeye girdikleri için hemen paslanırlar.
15 – Aktif olan metaller su ile de hemen tepkimeye girmek isterler. Bunun sonucu olarak da Hidrojen gazı açığa çıkar ve hidroksitler oluşur.