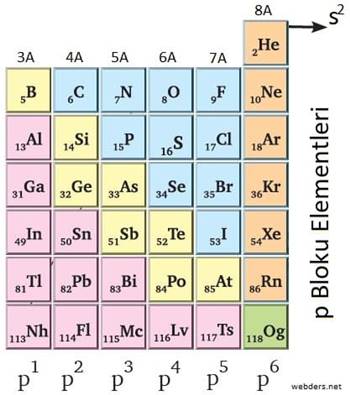
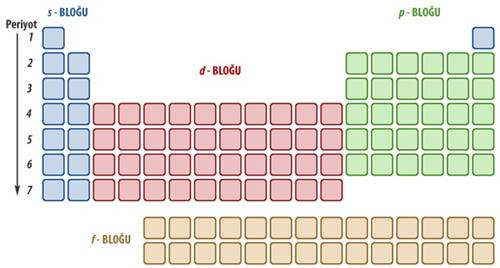
Periyodik Tablo P Bloku Elementleri ve Özellikleri
Elektron dizilimlerinin son orbitali p ile bitiyorsa bu elementlere P Bloku Elementleri denilir. 3A, 4A, 5A, 6A, 7A, 8A gruplarının tamamı (Helyum hariç) P bloku elementleridir. Bu bloktaki elementlerin değerlik orbitalleri s ve p şeklindedir. P blok elementleri metallerden, ametallerden ve soy gazlardan oluşur. Ametallerin tamamı bu bloktadır. Soy gazların ise Helyum hariç tamamı yine P blok elementleridir.
İlginizi Çekebilir: Periyodik Tablo 3A Grubu Elementleri
İlginizi Çekebilir: Periyodik Tablo 4A Grubu Elementleri
İlginizi Çekebilir: Periyodik Tablo 5A Grubu Elementleri
İlginizi Çekebilir: Periyodik Tablo 6A Grubu Elementleri
İlginizi Çekebilir: Periyodik Tablo 7A Grubu Elementleri
İlginizi Çekebilir: Periyodik Tablo 8A Grubu Elementleri
Periyodik Tablo P Bloku Elementlerinin Özellikleri
1 – Alüminyum, Galyum, İndiyum, Talyum, Nihonyum, Kalay, Kurşun, Flerovyum, Bizmut, Moskovyum, Livermoryum, Tennesin elementleri metal elementlerdir.
2 – Bor, Silisyum, Germanyum, Arsenik, Antimon, Tellur, Polonyum, Astatin elementleri yarı metal elementlerdir.
3 – Karbon, Azot, Fosfor, Oksijen, Kükürt, Selenyum, Flor, Klor, Brom, İyot elementleri ametal elementlerdir.
4 – Helyum elementi soy gaz olmasına rağmen elektron dizilimi s orbitali ile (s2) bitmektedir. Bu nedenle bazen S blok elementleri arasında bazen ise P blok elementleri arasında gösterilmektedir.
5 – Oganeson elementinin metal mi yoksa ametal mi konusunda henüz bir kesinlik yok.
6 – Soy gazlar dışında P blok elementleri arasında aynı periyotta soldan sağa doğru gidildikçe metalik karakter özelliği azalırken ametalik karakter özelliği artar.
7 – Soy gazlar dışında P blok elementleri arasında aynı periyotta yukarıdan aşağıya doğru gidildikçe metalik karakter özelliği artarken ametalik karakter özelliği azalır.
8 – En aktif ametal Flor elementidir.
9 – Bu bloktaki soy gazlar kararlı bir yapıya sahip oldukları için elektron alıp vermezler.
10 – 7A grubundaki elementler en aktif elementlerdir ve bunlara Halojenler denilir.
11 – Astatin radyoaktif özellik gösterirken diğer elementler doğada tuz yapısına katılırlar.
12 – Ametaller kendi ararlarında kovalent bağlar oluştururlar. Bunların Hidrojen ile bileşikleri asit özelliği gösterir.Ayrıca ametal oksitler tabiatta yaygın olarak bulunmaktadırlar.