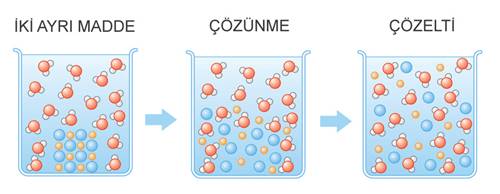
Çözeltilerde Derişim
Çözeltilerde derişim, bir çözeltideki çözünen madde miktarıdır. Bir kimya terimi olan derişim, birçok şekilde ifade edilebilir. Çözünen madde miktarı nitel olarak doymuş, doymamış, aşırı doymuş, seyreltik veya derişik ifadeleri kullanılırken nicel olarak kütlece, molce, hacimce ve sayıca derişim ifadeleri kullanılır. Bunların yanı sıra derişim, kütle, hacim ve mol gibi özelliklerin çözelti hacmine oranı şeklinde de (örneğin 100 gram su içinde 20 gram şekerin çözülmesiyle hazırlanan çözelti %20’lik çözeltidir) kullanılır.
Kütlece Yüzde Derişim (% Cm/m)
100 gram bir çözeltide çözünen maddenin gram cinsinden değerine denilir. Kütlece Yüzde Derişim ifadesi %Cm/m şeklinde gösterilir.
Formül:
%Cm/m = [ çözünen madde kütlesi / çözelti kütlesi ] * 100
Örnek:
140 gram su ve 60 gram şeker ile hazırlanmış çözeltinin kütle yüzde derişimi şöyledir:
%Cm/m = [60 / (140+60) ] * 100
%Cm/m = [60 / (200) ] * 100
%Cm/m = [0,3 ] * 100
%Cm/m = 30
Cevap: 140 gram su ve 60 gram şeker ile hazırlanmış çözeltinin kütle yüzde derişimi %30’dur.
Çözeltiyi Kütlece Seyreltme ve Deriştirme
Bir çözeltiye çözücü ekleyerek çözünen maddenin derişiminin azaltılması olayına seyreltme, bir çözeltideki çözücü miktarının azaltılarak çözünen maddenin derişiminin artırılması olayına ise deriştirme denir. Böyle bir durumda farklı formüller kullanmak gerekir.
1 – Eğer çözünen madde miktarı sabit (örneğin tuz) çözücü miktarı (örneğin su) değişiyorsa ise:
%C1 * m1 = %C2 * m2 formülü kullanılmalıdır.
Ama eğer aynı maddelerin (örneğin su ve tuz) farklı karışımları karıştırılıyorsa:
%Cson * mson = %C1 * m1 + %C2 * m3 + … + %Cn * mn formülü kullanılmalıdır.
Hacimce Yüzde Derişim (% CV/V)
Sıvı ve gaz karışımlarında hacimden faydalanılır. Bunun için hacimce yüzde derişimi formülleri geçerlidir. Hacimce yüzde derişim bir çözeltinin hacimce 100 biriminde çözünmüş olan maddenin aynı hacim biriminden değerine denir. Bu ifade %CV/V şeklinde gösterilir.
Formül:
%CV/V = [ çözünen madde hacmi / çözelti hacmi ] * 100
Örnek: olarak 160 ml su ile 40 ml etil alkol çözeltisini ele alalım. Buna göre:
%CV/V = [40 / (160+40) ] * 100
%Cm/m = [40 / (200) ] * 100
%Cm/m = [0,2 ] * 100
%Cm/m = 20
Cevap: 160 ml su ve 40 ml etil alkol ile hazırlanmış çözeltinin hacimce yüzde derişimi %20’dir.
Çözeltiyi Kütlece Seyreltme ve Deriştirme
Eğer çözeltide seyreltme veya deriştirme varsa:
%C1 * V1 = %C2 * V2 formülü kullanılmalıdır.
Eğer farklı miktarlarda aynı iki çözelti karışıtırılıyorsa:
%Cson * Vson = %C1 * V1 + %C2 * V3 + … + %Cn * Vn formülü kullanılmalıdır.
Kütle/Hacim Yüzde Derişim (% Cm/V)
Genellikle sıvı ve katı çözeltilerde bu derişim birimi kullanılır. Bir çözeltinin hacimce 100 biriminde çözünmüş olan maddenin kütlesinin değerine denir ve %Cm/V ile gösterilir.
Formül:
%Cm/V = [ çözünen madde miktarı / çözelti hacmi ] * 100
Örnek:
200 ml su ve 40 gram tuz ile hazırlanmış çözeltinin kütle/hacim yüzdesi şöyledir:
%Cm/V = [40 / (200) ] * 100
%Cm/m = [0,2 ] * 100
%Cm/m = 20
Cevap: 140 ml su ve 40 gram şeker ile hazırlanmış çözeltinin kütle/hacim yüzde derişimi %20’dir.
Milyonda Bir Kısım (ppm)
Genellikle karışımdaki çözünen madde miktarının çok az olduğu durumlarda kullanılan bir terimdir. Milyonda bir kısım, ppm ile gösterilir. Örneğin bir havuz suyunun 1.000.000 gramında 3 gram Klor elementi varsa Klor derişimi 3 ppm’dir. PPM derişimi ifadesi daha çok suların bileşimlerini belirtmede ve havadaki kirlilik yapan maddelerin derişimlerini belirtmede kullanılır.
Çözeltilerde Nitel Olma Durumu
Çözeltilerde çözünen maddenin miktarına göre durumlar söz konusudur. Bunlar doymuş çözelti, doymamış çözelti, aşırı doymuş çözelti, seyreltik çözelti ve derişik çözelti.
Doymamış Çözelti
Bir çözeltide çözücü madde çözebileceği madde miktarından daha azını çözmüş ise bu çözeltilere Doymamış Çözelti denir.
Doymuş Çözelti
Bir çözeltide çözücü madde çözebileceği en fazla madde miktarını çözmüş ise bu çözeltilere Doymuş Çözelti denir.
Aşırı Doymuş Çözelti
Bir çözeltide çözücü madde çözebileceği madde miktarından fazlasını çözmüş ise bu çözeltilere Aşırı Doymuş Çözelti denir.
Seyreltik Çözelti ve Derişik Çözelti
2 çözelti karşılaştırılırken içinde daha az çözülmüş madde bulunan çözeltiye Seyreltik Çözelti denir. 2 çözelti karşılaştırılırken içinde daha çok çözülmüş madde bulunan çözeltiye ise Derişik Çözelti denir. Ama bunlar 3. bir çözelti ile karşılaştırılır ise bu seyreltik ve derişik olan diğer çözeltilerin durumu değişir. Örnek olarak:
A) 1 adet şeker atılıp karıştırılmış bir bardak çay.
B) 2 adet şeker atılıp karıştırılmış bir bardak çay.
Yukarıdaki çözeltiler karşılaştırıldıklarında A çözeltisi Seyreltik Çözelti iken B çözeltisi Derişik Çözelti olur. Ama 2 çözelti:
C) 3 adet şeker atılıp karıştırılmış bir bardak çay.
yukarıdaki C çözeltisi ile karşılaştırıldıklarında bu kez A ve B çözeltileri Seyreltik Çözelti, C çözeltisi ise Derişik Çözelti olur.
Çözeltilerde Nicel Olma Durumu
Kütlece Derişim
Çözünen madde kütlesinin çözelti hacmine oranına Kütlece derişim denir. Birimi kg/m3.
Molce Derişim
Çözünmüş maddenin mol sayısının çözelti hacmine oranına Molce derişim denir. Birimi mol/m3. Aynı zamanda mol/L (= mol/dm3) de kullanılmaktadır.
Sayıca Derişim
Çözünme madde sayısının çözelti hacmine oranına Sayıca derişim denir. Birimi 1/m3.
Hacimce Derişim
Çözünmüş madde hacminin çözelti hacmine oranına Hacimce derişim denir. Birimi m3/m3.
Normalite
Molce derişimin eşdeğer etkene oranına Normalite denir. Eşdeğer etkenin tanımının kesin olmamasından dolayı IUPAC ve NIST normalitenin kullanımını desteklememektedir.
Molarite
Çözünenin mol sayısının çözücü kütlesine oranına Molarite denir. Birimi mol/kg.
Mol Kesri
Çözeltideki toplam mol sayısına oranına Mol kesri denir. Birimi mol/mol. Aynı zamanda çok küçük mol kesirleri için pp gösterimi (ppm, ppb) kullanılmaktadır.
Mol Oranı
Çözünenin mol sayısının diğer çözünmüş maddeler ve çözücü maddenin mol sayısına oranına Mol oranı denir.
Kütle Kesri
Çözünen kütlesinin çözelti kütlesine oranına Kütle kesri denir. Birimi kg/kg. Aynı zamanda çok küçük kütle kesirleri için pp gösterimi kullanılır.
Kütle Oranı
Çözünen kütlesinin diğer çözünenlerin ve çözücü kütlesine oranına Kütle oranı denir.