Brønsted-Lowry Asitler ve Bazları Teorisi
Johannes Nicolaus Brønsted ve Thomas Martin Lowry bilim insanları asit-baz tepkimesi kuramını açıklamışlardır. Ama bu açıklamaya kadar Arrhenius tanımı kabul ediliyordu. Bu nedenle Brønsted-Lowry teorisi, Arrhenius teorisinin genişletilmiş halidir. Brønsted-Lowry asit-baz teorisine göre asitler, H+ iyonu yani proton veren maddeler ve bazlar ise H+ iyonu yani proton alan maddelerdir.
*** H+ iyonu yani proton veren maddeler asittir:
HCl + H2O ↔ Cl– + H3O+
Asit + Baz ↔ Baz + Asit
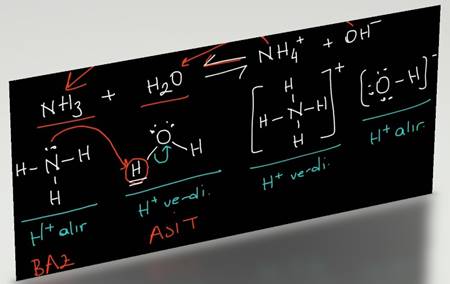
*** H+ iyonu yani proton alan maddeler bazdır:
NH3 + H2O ↔ NH4+ + OH–
Baz + Asit ↔ Asit + Baz
Daha önceden kabul edilen Arrhenius teorisine göre hidroksil grubu içeren maddeler baz idi ama Brønsted-Lowry teorisine göre H+ iyonu alan bütün maddeler bazdır. Dolayısıyla Arrhenius teorisine göre asit olan bütün maddeler Brønsted-Lowry teorisine göre de asittir.
Eşlenik Asit ve Eşlenik Baz
Bu teoriye göre asit-baz tepkimelerinde asit kendisinin eşlenik bazına dönüşürken baz ise kendisinin eşlenik asidine dönüşür. Yani:
asit + baz ![]() eşlenik baz + eşlenik asit
eşlenik baz + eşlenik asit