Bohr Atom Modeli Nedir?
1913 yılında Niels Henrik Bohr tarafından geliştirilen Bohr Atom Modeli, Rutherford Atom Modelinden yola çıkılarak geliştirilmiştir. Çünkü daha önce geliştirilen Dalton Atom Modeli, Thomson Atom Modeli ve Rutherford Atom Modeli artı (+, pozitif) yüklü parçacıkların bulunduğu atomda dairesel yörüngelerde elektronların dolaştığını belirtmişlerdi. Ama bu elektronların dolaştığı yörünge, hızları, momentumları hakkında bir sonuç elde edememişlerdi. Bohr atom modeli ise elektronların hareketleri üzerinde durdu.

Bohr atom modeline göre çekirdeğe en yakın elektron, kararlı ve ışık yaymaz. Ama elektrona yeterli enerji verilirse daha yüksek bir enerji seviyesine sıçrar ve dolayısıyla atom kararsız hale gelir. Atom kararlı hale gelmek için yani elektron tekrar aynı enerji seviyesine dönerken verilen enerji miktarı kadar enerji (foton, ışın taneciği, ışın dalgası) fırlatır.
“Okumak İster misiniz? Atom ile İlgilenen Bilim Adamları Kimlerdir?”
Bohr Atom Modelinin Varsayımları Nelerdir?
1 – Atomda bulunan elektronlar, çekirdekten belirli bir mesafede hareket ederler.
2 – Elektronların yörüngedeki açısal momentumları h/2*Pi sonucunun tam katlarıdır. (h = Planck sabiti)
3 – Atomun her kararlı halinin sabit bir enerjisi vardır.
4 – Kararlı enerjide elektronlar dairesel yörüngede (bu yörüngeye enerji düzeyleri, enerji kabukları denir) hareket ederler.
5 – Kararlı halde bulunan elektronlar ışık yaymazlar.
6 – Elektronlar, daha yüksek ışık seviyesinden daha düşük enerji seviyesine geçerken 2 seviye arasındaki enerji farkı kadar ışın dalgası yayarlar. Sonuç olarak E = E(son) – E(ilk) formülü ortaya çıkar.
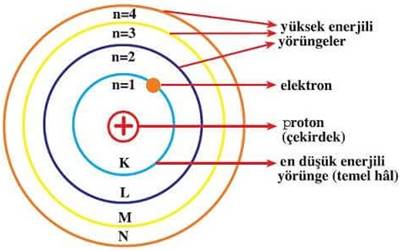
7 – Elektron hareketinin kararlı seviyeleri K, L, M, N, O gibi harflerle gösterilmektedir.
8 – En düşük enerji düzeyi 1 olmak üzere her enerji düzeyi +1 tam sayı ile belirlenir ve genel olarak “n” ile gösterilir. Yani n = 1, 2, 3, 4… gibi.
“Okumak İster misiniz? Atomu Kim İcat Etti? Atomu Bulan Bilim Adamı Kimdir? Atom Ne Zaman Bulundu?”
Bohr Atom Modelinin Eksikleri ve Yanlışları
Niels Henrik Bohr, elde ettiği bu sonuçlara rağmen geliştirdiği atom modelinin eksiklikleri ve yanlışları da vardı. Bunlar;
1 – Elektronlar çok hızlı hareket ettikleri için fiziğin yanı sıra izafiyet teorisi de göz önünde bulundurulmalı idi.
2 – Bohr atom modeli ise sadece tek elektronlu atomlar açıklanabilmekte. Çok elektronlu atomlar için kullanılamaz.
3 – Dalga-parçacık ikiliği göz önüne alınmamıştır.
4 – Heisenberg belirsizlik ilkesine göre yörünge kavramı yanlış.
5 – Nötronu keşfedememiştir. Nötronlar 1932 yılında James Chadwick tarafından keşfedilmiştir.
