Ayrışma ve Yer Değiştirme Reaksiyonları
Ayrışma ve Yer Değiştirme Reaksiyonları başlıklı yazımızda sizlere bu konuda detaylı bilgi vermeye çalışacağız. Eğer daha fazla bilgiye ihtiyacınız olursa sitemizde arama yaparak bu bilgilere ulaşabilirsiniz. Şimdi yazımıza geçelim. Kimyasal reaksiyonların çoğu dört sınıftan birine girer. Bu sınıfların ilki “birleşme reaksiyonu” adı altında açıklanan ve iki ayrı elementin birleşerek bir bileşik yaptığı reaksiyonların bulunduğu sınıftır. Bir başka reaksiyon da bir bileşiğin daha basit maddelere ayrılmasıdır (ayrışma reaksiyonu). Bu kısa girişten sonra şimdi konuyu biraz daha detaylandıralım isterseniz.
Ayrışma reaksiyonları:
Ayrışma ve Yer Değiştirme Reaksiyonları başlıklı yazımızda biraz daha detaya indiğimizde sizlere şunları aktarabiliriz. Bunlardan başka, biraz daha karışık elan iki reaksiyon vardır. Birincisinde bileşiğin içindeki bir iyon diğer bir iyonla yer değiştirir. Eğer gelen yeni iyon bir elementten sağlanıyorsa bu kimyasal değişmeye yer değiştirme reaksiyonu adı verilir. Yeni iyonun diğer bir bileşik tarafından sağlanması “çift yerdeğiştirme reaksiyonu” olarak bilinir. Bu adın takılmasının sebebi, reaksiyon sırasında iki bileşiğin de parçalanıp iyonların yer değiştirmesi sonucu iki yeni bileşik meydana getirmeleridir.
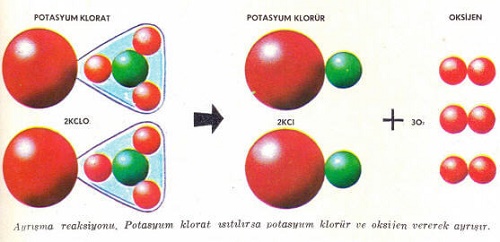
Kimya alanına ait Ayrışma ve Yer Değiştirme Reaksiyonları konusu hakkında daha fazla bilgiye sahip olabilirsiniz. Bunun için gerek sitemizden gerekse farklı kaynaklardan araştırma yapabilirsiniz. Yazımıza devam edecek olursak şunları da aktarabiliriz. Şimdi kaldığımız yerden devam edelim. Yazımıza şöyle devam edebiliriz. Bu çeşit reaksiyonlarda bir bileşik kendisinden daha basit olan maddelere ayrılır. Bu yeni maddeler bileşik veya element olabilir. Ayrışma reaksiyonunun olması için çoğu ısı (veya başka bir enerji) şart olduğundan, böyle kimyasal değişmeler bazen “ısı (ışık, elektrik vb.) etkisiyle ayrışma” reaksiyonları adıyla da tanınır. Biraz potasyum klorat kristalleri kuvvetlice ısıtılırsa oksijen gazı çıkar ve geriye potasyum klorür kalır. Laboratuvarda az miktarda oksijen lâzım olduğu zaman çoğu kere bu ayrıştırma reaksiyonu kullanılır. Reaksiyon sırasında potasyum klorata az miktarda manganezdioksit karıştırılırsa ayrışma daha düşük sıcaklıkta olur. Manganez dioksit katalizör olarak etkir. Son olarak bu konu hakkında geçmişte birçok araştırma yapıldığı gibi bundan sonra da araştırmalar yapılmaya devam edecek ve yeni bilgiler bizlere ulaştırılacaktır. Bilgiyle kalın…
