Atomlarda Elektron Alışverişi
Atomlarda Elektron Alışverişi başlıklı yazımızda sizlere bu konuda detaylı bilgi vermeye çalışacağız. Eğer daha fazla bilgiye ihtiyacınız olursa sitemizde arama yaparak bu bilgilere ulaşabilirsiniz. Şimdi yazımıza geçelim. Bu kısa girişten sonra şimdi konuyu biraz daha detaylandıralım isterseniz.
Atomlarda Elektron Alışverişi
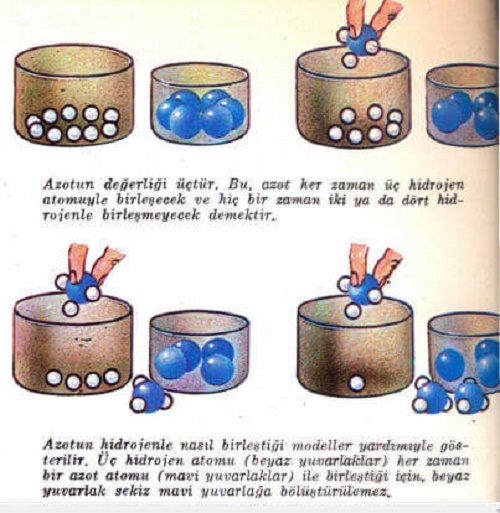
Atomlarda Elektron Alışverişi başlıklı yazımızda biraz daha detaya indiğimizde sizlere şunları aktarabiliriz. Atomlar bir araya gelerek bileşik moleküllerini yaparken belli oranlarda birleşirler. Örnek olarak, hidrojen klorla bileşik yaparken klor atomu her zaman bir hidrojen atomuyla birleşir, hiç bir zaman iki ya do üç hidrojen atomuyla birleşmez. Bu’ iki atomun birleşmesi sonunda bir hidrojen klorür (gaz hidroklorik asit) oluşur. Hidrojen oksijenle birleşerek su meydana getirirken, her zaman iki hidrojen atomuyla bir oksijen atomu birleşir. Eğer hidrojen azotla birleşerek amonyak yaparsa, her zaman üç hidrojen atomu bir azot atomuyla, yani 3’e 1 oranında birleşir. Eğer hidrojen karbonla metan (bataklık gazı) yaparsa, dört hidrojen atomu bir karbon atomuyla (yani 4’e 1 oranında) birleşecektir. Böylece değişik elementlerin atomları değişik sayıda hidrojen atomuyla birleşirler. Bir elementin birleştiği hidrojen atomu sayısına, o elementin değerliği denir. Bir klor atomu bir hidrojen atomuyla birleştiğinde, klorun değerliği birdir, oksijenin değerliği ikidir, çünkü bir oksijen atomu iki hidrojen atomuyla birleşir. Azotun değerliği üçtür, çünkü bir azot atomu üç hidrojen atomuyla birleşir. Karbonun değerliği ise dörttür, çünkü bir karbon atomu dört hidrojen atomuyla birleşir. Değerliği bir olan bir atom, değerliği bir olan bir başka atomla birleşebilir. Değerliği iki olan atom ya iki tane bir değerli ya da bir tane iki değerli atomla birleşir.
Kimya alanına ait Atomlarda Elektron Alışverişi konusu hakkında daha fazla bilgiye sahip olabilirsiniz. Bunun için gerek sitemizden gerekse farklı kaynaklardan araştırma yapabilirsiniz. Yazımıza devam edecek olursak şunları da aktarabiliriz. Şimdi kaldığımız yerden devam edelim. Yazımıza şöyle devam edebiliriz. Bir element atomunun birleşme yeteneği, aşağıda açıklandığı gibi yalnız alıp verdiği elektron sayısına bağlıdır. Bunun için, değerliğin temel birimi bir elektrondur. Hidrojen elementlerin-en basitidir, sadece bir elektronu vardır. Değerliğin «bir element atomuyla birleşen hidrojen sayısına eşit» olmasının bir nedeni de budur. Bir atomun niçin belli bir değerliğe sahip olduğunu anlamak için, atomların birleşme yollarını incelemek gerekir. Her atomun ortasında pozitif yüklü, oldukça ağır bir çekirdek bulunur. Çekirdeğin etrafında elektron denen negatif yüklü çok küçük tanecikler vardır. Bunlar çekirdek etrafında çok büyük hızla durmadan dönerler ve yörüngeleri bir kabuk meydana getirir. Dış kabukta bulunan elektronlar birleşmelerde etkin olurlar. Son olarak bu konu hakkında geçmişte birçok araştırma yapıldığı gibi bundan sonra da araştırmalar yapılmaya devam edecek ve yeni bilgiler bizlere ulaştırılacaktır. Bilgiyle kalın…
