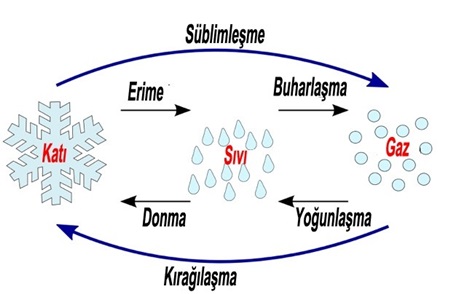
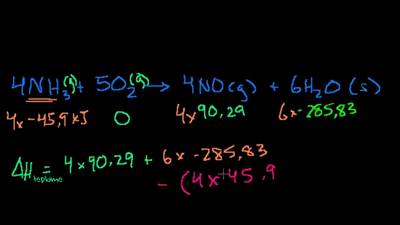Hess Yasası Nedir? Hess yasası, tepkime entalpisini hesaplamak için kullanılır. 1840 yılında Rus asıllı kimyacı ve fizikçi Germain Henri Hess tarafından yayınlandığı için bu ismi almıştır. Hess yasasına göre eğer bir tepkime, birden fazla aşamadan geçiyorsa bu tepkimedeki entalpi değişimi her aşamadaki entalpi değişimlerinin toplamına eşittir. Eğer tepkime entalpisi tam olarak ölçülemez ise daha önce […]
Hess Yasası Nedir?